30 CÂU HỎI
Kim loại có những tính chất vật lý chung nào sau đây?
A. Tính dẫn điện, tính dẫn nhiệt, có khối lượng riêng lớn, có ánh kim
B. Tính dẻo, có ánh kim, tính cứng
C. Tính dẻo, tính dẫn điện, tính dẫn nhiệt và có ánh kim
D. Tính dẻo, tính dẫn nhiệt, nhiệt độ nóng chảy cao
Ion kim loại nào sau đây có tính oxi hóa yếu nhất?
A. Fe3+.
B. Al3+.
C. Ag+.
D. Cu2+.
Ở điều kiện thường, chất nào sau đây tác dụng được với nước?
A. Na2CO3
B. Al2O3
C. CaO
D. Be
X là một kim loại nhẹ, màu trắng bạc, được ứng dụng rộng rãi trong đời sống. X là
A. Cu
B. Fe
C. Al
D. Ag
Dãy gồm các kim loại được xếp theo thứ tự tăng dần tính dẫn điện từ trái sang phải là
A. Fe, Cu, Al, Ag
B. Cu, Fe, Al, Ag
C. Ag, Cu, Al, Fe
D. Fe, Al, Cu, Ag
Criolit (Na3AlF6 hay 3NaF.AlF3) là nguyên liệu được dùng để sản xuất nhôm với mục đích:
1) Làm giảm nhiệt độ nóng chảy của Al2O3.
2) Tiết kiệm được năng lượng, tạo được chất lỏng có tính dẫn điện tốt hơn Al2O3.
3) Tạo chất lỏng có tỉ khối nhỏ hơn nhôm, nổi lên bề mặt nhôm ngăn cản nhôm nóng chảy bị oxi hoá
A. 1, 2
B. 2, 3
C. 1, 3
D. 1, 2, 3
Phát biểu nào sau đây không đúng?
A. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ ion Ca2+, Mg2+
B. Có thể điều chế nhôm bằng cách dùng khí CO khử Al2O3 ở nhiệt độ cao
C. Dung dịch HCl không làm mềm được nước cứng tạm thời
D. Trong các hợp chất, nguyên tố kim loại kiềm thổ chỉ có số oxi hóa là +2
Cho 3 gam hỗn hợp gồm Na và kim loại kiềm M tác dụng với nước. Để trung hoà dung dịch thu được cần 800 ml dung dịch HCl 0,25M. Kim loại M là
A. Li
B. Cs
C. K
D. Rb
Cho phảnứng oxi hóa – khử giữa Al và HNO3 tạo sản phẩm khử duy nhất là N2O. Tỉ lệ số phân tử HNO3 tạo muối với số phân tửHNO3 đóng vai trò chất oxi hóa là?
A. 1:6
B. 8:3
C. 4:1
D. 5:1
Trộn 50 ml dung dịch HCl 0,12M với 50 ml dung dịch NaOH 0,1M thu được dung dịch X. pH dung dịch X là
A. 7
B. 2
C. 10
D. 1
Cho m gam Mg vào dung dịch X gồm 0,03 mol Zn(NO3)2 và 0,05 mol Cu(NO3)2, sau một thời gian thu được 5,25 gam kim loại và dung dịch Y. Cho dung dịch NaOH vào, khối lượng kết tủa lớn nhất thu được là 6,67 gam. Giá trị của m là
A. 4,05
B. 2,86
C. 2,02
D. 3,60
Chocácchất:NaHCO3,CO,Al(OH)3,Fe(OH)3,HF,Cl2,NH4Cl.Sốchấttácdụngđượcvới dung dịch NaOH loãng ở nhiệt độthường là
A. 4
B. 5
C. 3
D. 6
Phương pháp nhiệt luyện thường dùng để điều chế các kim loại
A. hoạt động trung bình như Fe, Zn…
B. hoạt động mạnh như Ca, Na…
C. mọi kim loại như Cu, Na, Fe, Al…
D. kém hoạt động như Ag, Au…
Trong các kim loại sau, kim loại có nhiệt độ nóng chảy thấp nhất là
A. Cs
B. Li
C. Ba
D. Be
Thạch cao sống là chất nào sau đây?
A. CuSO4.5H2O
B. CaSO4
C. CaSO4. 2H2O
D. CaCO3
Hãy cho biết phản ứng nào sau đây không xảy ra ở điều kiện thường?
A. CaO + H2O → Ca(OH)2
B. 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
C. Be + 2H2O → Be(OH)2 + H2
D. Ba + 2H2O → Ba(OH)2 + H2
Cho 3,8 gam hỗn hợp muối M2CO3 và MHCO3 (M là kim loại kiềm) vào dung dịch H2SO4 2M (dư), sinh ra 0,496 lít khí (đktc). M là
A. K
B. Li
C. Rb
D. Na
Cho 8,52 gam hỗn hợp X gồm: Ca, MgO, Na2O tác dụng hết với 360 ml dung dịch HCl 1M (vừa đủ) thu được dung dịch Y. Khối lượng (gam) NaCl có trong Y là
A. 2,34
B. 8,75
C. 5,21
D. 7,02
Cho 3,36 lít CO2 ở đktc vào 200 ml dung dịch hỗn hợp NaOH 1M và Ba(OH)2 0,5M. Khối lượng kết tủa thu được sau phản ứng là
A. 9,85 gam
B. 19,7 gam
C. 14,775 gam
D. 1,97 gam
Dung dịch X gồm Na2CO3; K2CO3; NaHCO3. Chia X thành 2 phần bằng nhau:
- Phần 1 tác dụng với nước vôi trong dư thu được 20 gam kết tủa.
- Phần 2 tác dụng với dung dịch HCl dư thu được V lít khí CO2 ở đktc. Giá trị của V là
A. 2,24
B. 4,48
C. 6,72
D. 3,36
Trộn m gam Al với hỗn hợp A gồm Fe2O3, MgO và CuO, người ta thu được hỗn hợp X. Thực hiện phản ứng nhiệt nhôm hỗn hợp X trong điều kiện không có không khí, sau một thời gian thu được hỗn hợp Y. Hỗn hợp Y tan hoàn toàn trong dung dịch H2SO4 đặc nóng, sản phẩm khử thu được là 13,44 lít SO2duy nhất (đktc). Giá trị của m là
A. 2,7 gam
B. 5,4 gam
C. 10,8 gam
D. 21,6 gam
Một nguyên tố X thuộc chu kì nhỏ của bảng tuần hoàn các nguyên tố hóa học. X dễ dàng mất 3 electron tạo ra ion X3+ có cấu hình giống khí hiếm. Cấu hình electron của nguyên tử X là
A.1s22s22p6
B. 1s22s22p63s23p1
C.1s22s22p63s23p63d104s2
D.1s22s22p63s23p3
Dung dịch X gồm K2SO4 0,1M và Al2(SO4)3 0,12M. Cho rất từ từ dung dịch Ba(OH)2 vào 100 ml dung dịch X thì khối lượng kết tủa lớn nhất thu được là
A. 11,03
B. 10,94
C. 12,59
D. 11,82
Có các nhận xét sau:
(a) Kim loại mạnh luôn đẩy kim loại yếu hơn ra khỏi muối của nó.
(b) Những kim loại như Na, K, Ba, Ca chỉ có thể điều chế bằng cách điện phân nóng chảy.
(c) Tráng Sn lên sắt để sắt không bị ăn mòn là phương pháp bảo vệ kim loại bằng phương pháp điện hóa.
(d) Các kim loại kiềm có cùng kiểu cấu trúc mạng tinh thể.
(e) Hầu hết các hợp chất của kim loại kiềm đều tan tốt trong nước.
(f) Các muối của kim loại kiềm đều có môi trường trung tính.
(g) Kim loại kiềm được bảo quản bằng cách ngâm trong dầu hỏa.
Có bao nhiêu nhận xét đúng?
A. 3
B. 4
C. 2
D. 1
Thêm từ từ đến hết dung dịch chứa 0,2 mol KHCO3 và 0,1 mol K2CO3 vào dung dịch chứa 0,3 mol HCl. Thể tích CO2 thu được là
A. 3,36 lít
B. 5,04 lít
C. 4,48 lít
D. 6,72 lít
Sục CO2 vào dung dịch Ba(OH)2 ta quan sát hiện tượng theo đồ thị hình sau (số liệu tính theo đơn vị mol).
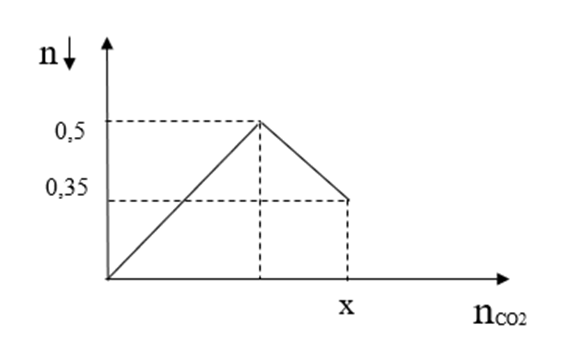
Giá trị của x là
A. 0,55 (mol)
B. 0,65 (mol)
C. 0,75 (mol)
D. 0,85 (mol)
KhiđiệnphândungdịchNaCl(cựcâmbằngsắt,cựcdươngbằngthanchì,màngngăn xốp) thì
A. ở cực âm xảy ra quá trình oxi hoá H2O và ở cực dương xảy ra quá trình khửCl-
B. ở cựcâm xảy ra quá trình khử Na+và ở cực dương xảy ra quá trình oxi hoáCl-
C. ở cực dương xảy ra quá trình oxi hoá Na+và ở cực âm xảy ra quá trình khửCl-
D. ở cực âm xảy ra quá trình khử H2O và ở cực dương xảy ra quá trình oxi hoá ionCl-
Điệnphân(vớiđiệncựctrơ) dung dịch muối sunfat của một kim loại hóa trị II với I = 3A. Sau 1930 giây điện phân thấy khối lượng catot tăng 1,92g. Kim loại đó là
A. Zn
B. Ba
C. Ca
D. Cu
Đốt cháy 2,15 gam hỗn hợp gồm Zn, Al và Mg trong khí oxi dư, thu được 3,43 gam hỗn hợp X. Cho X phản ứng vừa đủ với V ml dung dịch HCl 0,5M. Biết các phản ứng xảy ra hoàn toàn. Giá trị của V là
A. 160
B. 480
C. 240
D. 320
Điện phân dung dịch chứa 0,2 mol CuSO4và 0,12 mol NaCl bằng điện cực trơ, với cường độ dòng điện không đổi I = 5A trong thời gian 4632 giây thì dừng điện phân. Nhúng thanh Mg vào dung dịch sau điện phân, kết thúc phản ứng, khối lượng thanh Mg thay đổi như thế nào so với trước phản ứng. Giả thiết hiệu suất điện phân là100%.
A. giảm3,36gam
B. tăng3,20gam
C. không thay đổi
D. tăng1,76gam


