18 CÂU HỎI
Số nhóm carboxyl (-COOH) trong phân tử glutamic acid là
A. 4.
B. 1.
C. 3.
D. 2.
Chất nào sau đây có phản ứng màu biuret?
A. Glucose.
B. Triolein.
C. Aniline.
D. Albumin.
Amino acid X trong phân tử có một nhóm –NH2 và một nhóm –COOH. Cho 26,7 gam X phản ứng với lượng dư dung dịch HCl, thu được dung dịch chứa 37,65 gam muối. Công thức của X là
A. H2N-[CH2]3-COOH.
B. H2N-[CH2]2-COOH.
C.H2N-[CH2]4-COOH.
D. H2N-CH2-COOH.
Chất nào dưới đây thuộc loại polymer?
A. Glucose.
B. Fructose.
C. Saccharose.
D. Cellulose.
Cho polymer thiên nhiên X được lấy từ mủ cây cao su, có công thức cấu tạo như sau:

Bằng phương pháp hoá học có thể tổng hợp được X bằng phản ứng trùng hợp từ
A. 2-methylbuta-1,3-diene.
B. buta-1,3-diene.
C. propylene.
D. 2-methylbutane.
Trong công nghiệp, người ta có thể điều chế poly(vinyl alcohol) bằng cách đun nóng PVC trong dung dịch kiềm. Khi đó xảy ra phản ứng sau:
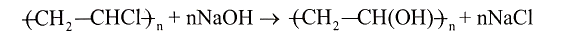
Phản ứng trên thuộc loại phản ứng
A. giữ nguyên mạch polymer.
B. phân cắt mạch polymer.
C. oxi hoá - khử.
D. tăng mạch polymer.
Tơ nào sau đây được sản xuất từ cellulose?
A. Tơ nitron.
B. Tơ capron.
C. Tơ visco.
D. Tơ nylon-6,6.
Poly(ethylen terephthalate) được điều chế bằng phản ứng với terephthalic acid với chất nào sau đây?
A. Ethylene glycol.
B. Ethylene.
C. Glycerol.
D. Ethyl alcohol.
Polymer Z được tổng hợp theo phương trình hoá học sau:
Polymer Z được điều chế bằng phản ứng
A. trùng hợp.
B. trùng ngưng.
C. thế.
D. trao đổi.
Cao su buna-S (hay còn gọi là cao su SBR) là loại cao su tổng hợp được sử dụng rất phổ biến, ước tính 50% lốp xe được làm từ SBR. Thực hiện phản ứng trùng hợp các chất nào dưới đây thu được sản phẩm là cao su buna-S?
A. CH2=CHCH=CH2 và C6H5CH=CH2.
B. CH2=CHCH=CH2 và sulfur.
C. CH2=CHCH=CH2 và CH2=CHCl.
D. CH2=CHCH=CH2 và CH2=CHCN.
Kí hiệu cặp oxi hoá - khử ứng với quá trình khử:Fe3++3e→Felà
A. Fe3+/Fe2+.
B. Fe2+/Fe.
C. Fe3+/Fe.
D. Fe2+/Fe3+.
Sức điện động chuẩn của pin Galvani được tính như thế nào?
A. Bằng hiệu của thế điện cực chuẩn tương ứng của điện cực dương và điện cực âm.
B. Bằng tổng của thế điện cực chuẩn tương ứng của điện cực dương và điện cực âm.
C. Bằng tích của thế điện cực chuẩn tương ứng của điện cực dương và điện cực âm.
D. Bằng thương của thế điện cực chuẩn tương ứng của điện cực dương và điện cực âm.
Cặp oxi hoá- khử nào sau đây có giá trị thế điện cực chuẩn lớn hơn 0?
A. K+/K.
B. Li+/Li.
C. Ba2+/Ba.
D. Cu2+/Cu.
Cho các cặp oxi hoá-khử của kimloại và thế điện cực chuẩn tương ứng:
|
Cặp oxi hoá - khử |
Na+/Na |
Ca2+/Ca |
Ni2+/Ni |
Au3+/Au |
|
Thế điện cực chuẩn (V) |
-2,713 |
-2,84 |
-0,257 |
+1,52 |
Trong các kim loại trên, số kim loại tác dụng được với dung dịch HCl ở điều kiện chuẩn, giải phóng khí H2 là
A. 1.
B. 4.
C. 2.
D. 3.
Cho thứ tự sắp xếp một số cặp oxi hoá – khử trong dãy điện hoá: Al3+/Al, Fe2+/Fe, Sn2+/Sn, Cu2+/Cu.Kim loại nào sau đây có phản ứng với dung dịch muối tương ứng?
A. Fe và CuSO4.
B. Fe vàAl2(SO4)3.
C. Sn và FeSO4.
D. Cu và SnSO4.
Một pin điện hoá có điện cực Zn nhúng trong dung dịch ZnSO4 và điện cực Cu nhúng trong dung dịch CuSO4. Sau một thời gian pin đó phóng điện thì
A. khối lượng điện cực Zn giảm còn khối lượng điện cực Cu tăng.
B.khối lượng điện cực Zn tăng còn khối lượng điện cực Cu giảm.
C. khối lượng cả hai điện cực Zn và Cu đều tăng.
D. khối lượng cả hai điện cực Zn và Cu đều giảm.
Thế điện cực chuẩn của các cặp oxihoá-khử của kim loại M+/M và R2+/R lần lượt là +0,799 V và +0,34 V. Nhận xét nào sau đây là đúng ở điều kiện chuẩn?
A. M có tính khử mạnh hơn R.
B. M+có tính oxihoá yếu hơn R2+.
C. M khử được ion H+ thành H2.
D. R khử được ion M+ thành M.
Thiết lập pin điện hóa ở điều kiện chuẩn gồm hai điện cực tạo bởi các cặp oxi hóa – khử Ni2+/Ni () và Cd2+/Cd . Sức điện động chuẩn của pin điện hoá trên là
A. +0,146 V.
B. 0,000 V.
C. -0,146 V.
D. +0,660 V.

