18 CÂU HỎI
Phần I: Câu trắc nghiệm nhiều phương án lựa chọn. Thí sinh trả lời từ câu 1 đến câu 18. Mỗi câu hỏi thí sinh chỉ chọn một phương án.
Insulin là hoocmon của cơ thể có tác dụng điều tiết lượng đường trong máu. Thủy phân một phần insulin thu được heptapeptide (X). Khi thủy phân không hoàn toàn X thu được hỗn hợp các peptide trong đó có các peptide sau: Ser-His-Leu; Val-Glu-Ala; His-Leu-Val; Gly-Ser-His. Nếu đánh số amino acid đầu N trong X là số 1 thì amino acid Val sẽ ở vị trí số
A. 3.
B. 5.
C. 2.
D. 4.
Kí hiệu cặp oxi hoá - khử ứng với quá trình khử: Fe3+ + 1e → Fe2+ là
A. Fe2+/Fe.
B. Fe3+/Fe.
C. Fe3+/Fe2+.
D. Fe2+/Fe3+.
Điện phân dung dịch AgNO3 với anode và cathode trơ. Quá trình xảy ra ở cathode tại giai đoạn đầu của phản ứng điện phân là
A. 2H2O(l) → O2(g) + 4H+(aq) + 4e.
B. 2H2O(l) + 2e → H2(g) + 2OH- (aq).
C. Ag+(aq) + e → Ag(s).
D. Ag(s) → Ag+(aq) + e.
Số đồng phân alkene có công thức phân tử C4H8 là
A. 4.
B. 3.
C. 6.
D. 5.
Trong số các ion: Ag+, Al3+, Fe2+, Cu2+, ion nào có tính oxi hoá mạnh nhất ở điều kiện chuẩn?
A. Ag+.
B. Fe2+.
C. Cu2+.
D. Al3+.
Ester nào sau đây khi thủy phân trong môi trường kiềm cho muối acetate?
A. C2H5COOCH3.
B. HCOOC2H5.
C. HCOOCH3.
D. CH3COOCH3.
Tinh bột và cellulose là các polymer tự nhiên tạo bởi các mắt xích tương ứng là
A. α-fructose và β-glucose.
B. β-fructose và β-glucose.
C. α-glucose và β-fructose.
D. α-glucose và β-glucose.
Trong công nghiệp, nhôm được sản xuất từ quặng bauxite theo 2 giai đoạn chính:
- Giai đoạn 1: Tinh chế quặng bauxite.
- Giai đoạn 2: Điện phân Al2O3 nóng chảy (Al2O3 được trộn cùng với cryolite Na3AlF6).
Sản phẩm điện phân ở cathode là nhôm (lỏng) và ở anode là hỗn hợp khí CO2, CO. Cấu tạo bể điện phân như hình sau:
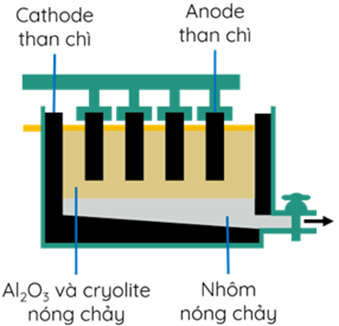
Sau một thời gian điện phân thu được 5,4 tấn Al tại cathode và hỗn hợp khí tại anode gồm CO2 (chiếm 80% theo thể tích) và CO (chiếm 20% theo thể tích). Giả thiết không có thêm sản phẩm nào được sinh ra trong quá trình điện phân. Khi đó khối lượng carbon bị oxi hóa trên anode là bao nhiêu tấn?
A. 3,1.
B. 2,0.
C. 0,8.
D. 1,6.
Công thức phân tử của glucose là
A. C6H12O6.
B. C12H22O6.
C. C12H22O11.
D. C6H10O5.
Tên viết tắt của peptide: HOOC-CH2-NH-CO-CH(CH3)NH2 là
A. Ala-Val.
B. Gly-Ala.
C. Ala-Gly.
D. Val-Ala.
X là kim loại có tính cứng lớn nhất trong các kim loại nên được mạ bên ngoài các sản phẩm để bảo vệ sản phẩm và hạn chế sự mài mòn (như hình bên).

X là kim loại nào sau đây ?
A. W.
B. Cr.
C. Os.
D. Cs.
Những polymer nào sau đây thuộc loại polymer thiên nhiên ?
A. Tơ tằm, tinh bột và cellulose.
B. Tơ capron, tinh bột, cellulose.
C. Tơ capron, polystyrene, tinh bột và cellulose.
D. Tơ capron, polystyrene.
Phản ứng của ethylene với HBr tuân theo cơ chế :
A. thế electrophile.
B. cộng electrophile.
C. cộng nucleophile.
D. thế nucleophile.
Cho hợp chất thơm m-HO-C6H4-CH2OH tác dụng với dung dịch NaOH dư. Sản phẩm hữu cơ tạo ra là :
A. m-HO-C6H4-CH2ONa.
B. m-NaO-C6H4-CH2OH.
C. m-NaO-C6H4-CH2ONa.
D. p-NaO-C6H4-CH2OH.
Khi thay thế một nguyên tử hydrogen trong ammonia bằng một gốc hydrocarbon ta thu được hợp chất amine bậc mấy ?
A. 2.
B. 4.
C. 1.
D. 3.
Cho biết số thứ tự của Mg trong bảng tuần hoàn là 12. Vị trí của Mg trong bảng tuần hoàn là :
A. chu kì 3, nhóm IIA.
B. chu kì 2, nhóm IIB.
C. chu kì 3, nhóm IIIA.
D. chu kì 3, nhóm IIIB.
Quá trình đốt cháy ethanol diễn ra theo phản ứng: C2H5OH(l) + 3O2(g) → 2CO2(g) + 3H2O(l)
Cho các giá trị năng lượng liên kết sau: EC–C = 347 kJ/mol; EO=O = 496 kJ/mol; EC–O = 336 kJ/mol; EC–H = 410 kJ/mol; EC=O = 805 kJ/mol; EO–H = 465 kJ/mol. Giá trị Δr của phản ứng trên là :
A. –1324 kJ.
B. 1324 kJ.
C. –1671 kJ.
D. 1671 kJ.
Trong định nghĩa về liên kết kim loại: “Liên kết kim loại là liên kết hình thành do lực hút tĩnh điện giữa các electron hóa trị.(1). với các ion.(2). kim loại ở các nút mạng”.
Các từ cần điền vào vị trí (1), (2) lần lượt là :
A. hoá trị, âm.
B. ngoài cùng, dương.
C. tự do, dương.
D. hoá trị, lưỡng cực.

